
第51回日本産科婦人科学会学術講演会 シンポジウム報告
シンポジウム2 母児間免疫応答の異常
「抗リン脂質抗体症候群における母児相関 ~免疫学的血液凝固異常を中心に~」
演者 東海大学医学部産婦人科学教室 杉 俊隆
*青字は私自身が特に重要と感じた部分です。
以前よりSLEをはじめとする自己免疫疾患の中に不育症が数多く含まれることが知られ、母体の免疫能の異常が着床や妊娠維持に障害を起こす可能性が指摘されてきた。最近になって、それが抗リン脂質抗体という自己抗体によって惹き起こされるという説が注目されるようになり、抗リン脂質抗体と関連する不育症、反復血栓症、血小板減少症をまとめて抗リン脂質抗体症候群と称し、広く認知されるようになった。不育症とならんで血栓、止血関係の疾患がその症候群の診断基準案に列挙されたということは、不育症の病因として免疫だけではなく、免疫・血液学的機序が存在する可能性が示唆されたことになる。
抗リン脂質抗体の中でも抗カルジオリピン抗体やループスアンチコアグラントなどの陰性荷電のリン脂質に対する抗体の目標抗原はリン脂質そのものではなく、リン脂質に結合したβ2-glycoprotein I (β2GPI )やプロトロンビンであることが最近解明された。しかしながら、それ以外の未知の抗リン脂質抗体も多く存在すると推察されている。血栓と関係の深い血小板や血管内皮細胞の細胞膜外層には、陰性荷電のリン脂質はほとんどなく、電気的中性のリン脂質が多くを占めており、無視することはできない。そこで本研究では、電気的中性のリン脂質であるフォスファチジルエタノールアミン(PE)に対する抗体に注目して研究を進めてきたが、抗PE抗体の多くもまた、抗カルジオリピン抗体と同様リン脂質そのものを認識するのではなく、PEに結合する蛋白を認識すること、そしてその蛋白はキニノーゲンであると言うことを内外で初めて解明し発表した。
キニノーゲンは内因系血液凝固因子の一つであり、凝固線溶にきわめて重要な役割をもつだけではなく、女性生殖器に非常に高濃度で存在し、ブラジキニンを放出することにより、カリクレイン-キニン系を介して妊娠分娩に重要な役割を持つ可能性が示唆されている。したがって、キニノーゲンを認識する抗リン脂質抗体が不育症の原因になるという仮説は十分有り得る。さらに、最近では同じカリクレイン-キニン系に属する血液凝固第12因子の欠乏も抗リン脂質抗体とならんで不育症の重要な原因の一つとして報告されており、カリクレイン-キニン系の破綻という新しい不育症の原因が明らかになりつつある。
抗リン脂質抗体とは
抗リン脂質抗体とはリン脂質に対する自己抗体であり、具体的には電気的陰性のリン脂質(カルジオリピン、フォスファチジルセリン、フォスファチジルグリセロール、フォスファチジルイノシトール、フォスファチジン酸など)や、電気的中性のリン脂質(フォスファチジルエタノールアミン、フォスファチジルコリン)に対する抗体である。しかしながら、従来は名前どおりリン脂質を認識する抗体であると思われてきたが、最近、その多くは、実はリン脂質そのものを認識する抗体ではなく、リン脂質に結合する血漿蛋白に対する抗体であるということが分かってきた。一番最初に発見された抗原は、β2GPIであり、当初はコファクターと称されたが、その後は事実上の抗カルジオリピン抗体の目標抗原ということでコンセンサスが得られている。次いで、ループスアンチコアグラントの目標抗原としてプロトロンビンが報告された。これらは、カルジオリピンやフォスファチジルセリンなど、電気的陰性のリン脂質に対する抗体の対応抗原である。その後我々は、中性のリン脂質であるフォスファチジルエタノールアミン(PE)に対する抗体も同様にリン脂質結合蛋白を認識することを発見し、それがキニノーゲンであることを同定した。このように、抗リン脂質抗体といっても実は全く異なる抗体の総称であり、共通点はリン脂質に結合する蛋白を認識するということだけである。したがって、それぞれの病原性およびその機序は目標抗原によって異なると考えられる(表1)。
表1 抗リン脂質抗体の対抗抗原
・β2ーグリコプロテイン I
・プロトロンビン
・キニノーゲン
・プロテイン C (?)
・プロテイン S (?)
・トロンボモジュリン (?)
・アネキシン (?)
・酸化LDL (?)
・トロンボキサン A2 (?)
近年、抗リン脂質抗体と不育症、反復血栓症、血小板減少症との関係は広く知られており、注目を浴びている。特に、後天的な血栓傾向の原因としては、最も重要なものの一つであると位置付けられるようになった。抗リン脂質抗体症候群は、関連する全身疾患をもたないprimary抗リン脂質抗体症候群と、SLEやその他の膠原病を伴うsecondary抗リン脂質抗体症候群に分けられる。抗リン脂質抗体症候群に関連する合併症には、静脈血栓、動脈血栓、流早産、血小板減少が代表的である。妊娠に関しては、妊娠中期以降の子宮内胎児死亡がもっとも抗リン脂質抗体に特異的である。胎盤の血栓が原因と言われているが、因果関係は未だ不明である。また、妊娠初期の反復流産も抗リン脂質抗体と関係している。
抗リン脂質抗体は当初、梅毒血清反応の生物学的偽陽性として検出された。ワッセルマン反応において、抗原としてカルジオリピンを用いていたため、陽性というのはすなわち抗カルジオリピン抗体を意味していた訳である。このような歴史的な流れより、今でも抗リン脂質抗体といえばカルジオリピンやフォスファチジルセリンなど陰性荷電のリン脂質に対する抗体を指す事が多い。しかしながら、カルジオリピンは心臓のミトコンドリア膜に存在し、血小板や血管内皮細胞の細胞膜には存在しない。さらに、血管内皮細胞や血小板などの細胞膜外層には、restingな状態ではフォスファチジルセリンなどの陰性荷電のリン脂質はほとんど存在せず、活性化してはじめて出現する。したがってrestingな血小板にはβ2GPIも結合できず、それを認識する抗体が血小板を刺激して活性化、凝集させ、血栓を惹き起こすという仮説には多少無理がある。一方、中性のリン脂質であるPEやフォスファチジルコリンは、常に細胞膜外層に存在し、その主要構成成分である。したがって、それらを認識する抗体を無視することはできない。にもかかわらず、中性リン脂質に対する抗体に関する報告は比較的少ない。その理由は、多くの施設でそれらの抗体の測定をしていないという事と、していたとしても、不適切な測定法による偽陰性のため頻度が少ないと誤解されているためと思われる。
そこで、我々は抗PE抗体に焦点をあてて研究を進めてきた。
新しい抗リン脂質抗体の特異性
我々は既に抗PE抗体の多くがPEそのものではなく、PEに結合した血漿蛋白を認識すること、その血漿蛋白はキニノーゲンおよびその結合蛋白である11因子とプレカリクレインであることを報告した(図1)。抗PE抗体はキニノーゲンを単独では認識せず、PEに結合したキニノーゲンのみを認識した。このことより、キニノーゲンがPEに結合すると特異的な立体構造の変化が生じ、新しいエピトープが出現し、それを抗PE抗体が認識することが示唆された。また、キニノーゲンはPE以外のリン脂質(カルジオリピン、フォスファチジルセリン、フォスファチジルコリン)にも結合したが、他のリン脂質に結合した場合、抗PE抗体はキニノーゲンを認識しなかった。これは、PEのみが特異的な立体構造の変化をキニノーゲンに惹き起こし、抗PE抗体が認識するエピトープを出現させると考えられる。
図1. 抗PE抗体の目標抗原

キニノーゲンのうち高分子キニノーゲンは血液凝固因子であり、活性化すると立体構造変化のため抗原性が変わってしまう。また、一般によくELISAに用いられるウシ胎児血清にはキニノーゲンは大人の半分以下しか含まれていない。さらに、これらのウシ血清は培養用に売られている事が多く、フィルターを通してある事が多いが、その操作により、キニノーゲンをはじめとするcontact activationに関わる血液凝固因子はかなり除去される可能性がある。以上の理由で従来のウシ血清を用いたELISA法では、結果はウシ血清の品質に左右され、正しい結果が得られないことが多い。我々は血清の変わりに血漿を用いることによってintactのキニノーゲンをELISAの系に加え、安定したデータを得ている。また、陽性にでた抗体はさらに精製したキニノーゲンを用いて対応抗原の確認を行っている。
このように、抗PE抗体の対応抗原がキニノーゲンであるということが解明されたために、安定した抗PE抗体ELISAが確立でき、それを用いて不育症患者に対して抗PE抗体のスクリーニングを施行した。その結果、初期流産(妊娠10週未満)を繰り返す不育症群の抗PE抗体陽性率は正常群と比較して有意に多く(p=0.0002)、PE結合蛋白を認識する抗PE抗体、PEそのものを認識する抗PE抗体あわせて31.7%となった(表2、3)。また、精製したキニノーゲンを用いてPE結合蛋白を認識する抗PE抗体の対応抗原を検討したところ、73.3%がPEに結合したキニノーゲンを認識した。
表2.妊娠初期反復流産患者における抗PE抗体
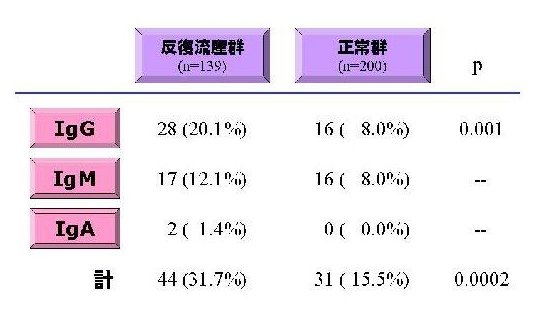
表3.妊娠初期反復流産患者における抗PE抗体IgG

これに対して、従来より検査されている陰性荷電のリン脂質に対する抗体である抗カルジオリピン抗体、抗フォスファチジルセリン抗体、ループスアンチコアグラントなどを初期流産(妊娠10週未満)を繰り返す不育症群に対してスクリーニングしたところ、正常群と比較して陽性率に差を認めなかった。
新しい抗リン脂質抗体の病原性
キニノーゲンは血液凝固反応のうち内因系に属する凝固因子であり、高分子キニノーゲン、プレカリクレイン、第11因子、第12因子の4つの蛋白をcontact proteinという。この4つの蛋白が陰性荷電の表面に集合し、内因系の血液凝固反応が開始される。しかしながら、in vitroではこれらの蛋白が欠損しているとaPTTは延長するが、in vivoではこれらの蛋白は抗凝固、線溶促進作用があり、欠損すると出血傾向ではなく血栓の原因となり得ることがわかってきた。たとえば血小板に対しては、キニノーゲンは血小板に結合してそのトロンビンによる活性化、凝集を抑制していることがわかっている。その血小板活性化を抑制する活性はキニノーゲンのドメイン2と3にある。我々は、キニノーゲンを認識する抗PE抗体が血小板上のキニノーゲンを認識することにより、キニノーゲンの血小板活性化抑制作用を阻害し、血栓の原因になるのではないかと考え、in vitroで血小板凝集能にて検討した。その結果、キニノーゲンを認識する抗PE抗体は、キニノーゲンを認識しない抗PE抗体と比較して著明にトロンビン惹起性血小板凝集能を亢進させた。
以上の結果より、抗PE抗体はキニノーゲン、ドメイン2、3を認識する可能性が示唆されたので、合成ペプチドを作成してmappingを施行したところ、この抗体はキニノーゲン、ドメイン2、3に存在するcystein protease inhibitor部位(QVVAG)や、ドメイン3のCys333-Cys352を認識する事が明らかとなった。QVVAGは血小板のcalpainを阻害し、トロンビン惹起性血小板凝集能を抑制する部位として知られている。このことより、キニノーゲン依存性抗PE抗体陽性の不育症患者には、抗血小板療法である低用量アスピリン療法が有効である可能性が示唆された。また、不育症患者に対して血小板凝集能のスクリーニングを行った結果、正常群と比較して血小板凝集能がin vivoでも有意に(p=0.0001)亢進していることが確認された。
不育症群と正常群で抗核抗体をスクリーニングしたところ、正常群では13%、不育症群では22.3%、抗PE抗体陽性不育症群では35.7%が陽性(≧80×)であり、抗リン脂質抗体が陽性の患者は抗核抗体陽性率が高かった(図2)。しかしながら、正常群でも13%に陽性にでているので、抗核抗体が陽性と言うだけで安易に抗リン脂質抗体症候群に準じた治療をするのは、疑問である。また、フローサイトメーターを用いて末梢血リンパ球の表面マーカーを検討したところ、抗PE抗体陽性不育症は正常群、原因不明不育症群と比較して活性化T細胞(CD4+DR+、CD8+DR+)が多い傾向にあった。これらのことより、抗PE抗体陽性患者は全身性に免疫のバランスが崩れていると考えられ、流産の結果として誘導されたというよりは、自己免疫疾患の一つとして誘導され、流産の原因となっていると考えたほうが説得力がある。抗PE抗体がキニノーゲンの抗血栓活性のある部位を認識するという我々のデータもこの仮説を支持している。
図2.不育症患者における抗核抗体
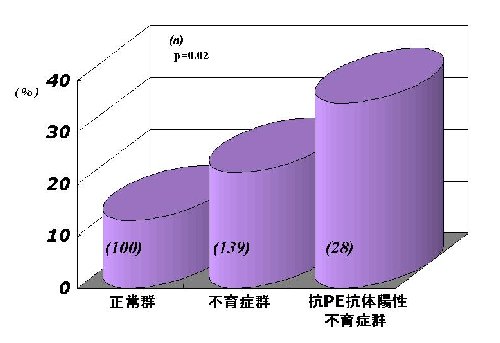
カリクレイン-キニン系と生殖
キニノーゲンは、血液凝固反応の内因系の一員であるだけでなく、カリクレインーキニン系においてキニンを放出する重要な蛋白でもある。カリクレイン-キニン系を概説すると、活性化第12因子がプレカリクレインをカリクレインにし、カリクレインはキニノーゲンを切断してブラジキニンを放出させる。ブラジキニンは血管内皮細胞を刺激して組織プラスミノーゲンアクチベーター(tPA)を分泌させ(図3)、線溶系を活性化させるとともに(図4)、胎盤血流の調節に関与している。最近になって、キニノーゲンは子宮胎盤ユニットに高濃度に蓄積しており、妊娠中に周期的に変動していること、カリクレイン-キニン系は種々の物質や代謝産物の経胎盤輸送や胎盤血流の調節に関与していることなどが相次いで報告され、その妊娠維持における重要性が注目されている。したがって、我々が発見したキニノーゲンを認識する抗PE抗体が流産の原因になるという仮説は、非常に合理的であると考えられる。
図3.カリクレインーキニン系
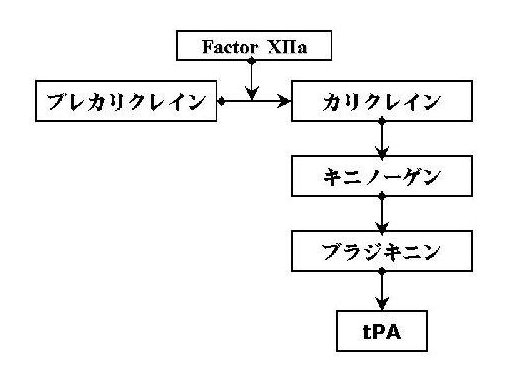
図4.線溶系
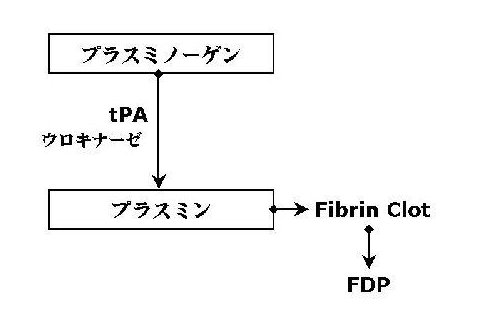
カリクレイン-キニン系の破綻と不育症
我々はすでにカリクレイン-キニン系の蛋白の一員であるキニノーゲンまたはキニノーゲンの結合蛋白である第11因子とプレカリクレインを認識する抗リン脂質抗体が、初期流産を繰り返す不育症に多いことを報告した。そこで、不育症患者においてカリクレイン-キニン系関連蛋白を中心とした血液凝固系のスクリーニングを施行したところ、抗リン脂質抗体症候群とならんで、第12因子活性低下が2大要因として挙げられた。抗リン脂質抗体の多くはキニノーゲンを認識する抗PE抗体であったので、結局は両方ともキニノーゲン-キニン系に関する要因であった。両者に共通であったのは、妊娠初期(10週未満)に流産を繰り返すということであり、妊娠中期以降の子宮内胎児死亡が特徴的な抗カルジオリピン抗体やループスアンチコアグラント陽性例とは異なる。
Grisらは、原因不明反復初期流産患者に対して第12因子の定量をスクリーニングしたところ、9.4%の患者に第12因子欠乏があると報告した。同様に我々も反復流産患者171名に対して第12因子の活性を検討したところ、15.8%に活性低下(60%未満)がみられた。またGallimoreらは抗リン脂質抗体陽性患者のうち20.9%に第12因子欠乏があると報告した。それらの患者の中には第12因子を認識する抗体が高頻度に見い出され、自己抗体を介する第12因子欠乏という可能性が示唆された。我々の検討でも、第12因子活性低下例の37.0%は抗リン脂質抗体陽性であった。
新しい抗リン脂質抗体症候群
従来、抗リン脂質抗体に関する研究のほとんどは抗カルジオリピン抗体に関するものであった。しかしながら、それは単に歴史的に梅毒血清反応にカルジオリピンが用いられていたために、伝統としてカルジオリピンが注目されていたにすぎず、その血栓、流産との因果関係、病原性もいまだ解明されるに至っていない。
本研究では中性のリン脂質であるPEに注目し、抗PE抗体の事実上の目標抗原としてキニノーゲンを内外で初めて特定した。これは、抗リン脂質抗体の目標抗原としては、抗カルジオリピン抗体のβ2GPI 、ループスアンチコアグラントのプロトロンビンに次いで3番目に発見されたものである。さらに、妊娠初期反復流産と抗PE抗体との非常に強い相関関係が示され、キニノーゲンを認識する抗PE抗体の血小板に対する病原性もin vitroで証明され、低用量アスピリン療法という具体的な治療法も示唆された。キニノーゲンは血液凝固因子であるが、欠損すると血栓症になることが知られている。女性生殖器に豊富に存在し、妊娠維持や分娩に関与することが指摘されており、凝固、線溶のみならず、カリクレイン-キニン系の一員として生殖にも非常に重要な役割を果たしている。また、キニノーゲンと同様カリクレイン-キニン系の一員である第12因子の欠乏という新しい不育症の要因も解明された。この第12因子欠乏もまた抗リン脂質抗体との関係が報告され、キニノーゲンを認識する抗PE抗体と同様、第12因子を認識する抗体の存在が報告されている。これらはいずれもカリクレイン-キニン系蛋白を認識し、破綻させることにより流産を惹き起こす原因としてまとめることができる。その特徴は、妊娠初期流産を惹き起こすことである。
いままで原因不明不育症は約40%にのぼると言われているが、この新しい症候群はあわせて20-30%にのぼると考えられ、原因不明不育症の多くが説明可能になると期待される。また従来は原因不明例に夫リンパ球を用いた免疫療法などが行われていたが、このことにより免疫療法の適応がさらに適切になることが期待される。
共同研究者
内田能安、勝沼潤子、善方菊夫、松林秀彦、鈴木隆弘、和泉俊一郎、岩崎克彦、牧野恒久、John A. McIntyre (Methodist Hospital of Indiana, USA)